Передумови та дизайн дослідження
Ретатрутид (LY3437943) – це новий однопептидний препарат, який активуєтри рецептори одночасно: ГІП, ГПП-1 та глюкагон. Для оцінки його ефективності та безпеки у осіб з ожирінням, але без діабету, було проведено рандомізоване, подвійне сліпе, плацебо-контрольоване дослідження фази 2 (NCT04881760). Загалом338 учасниківз ІМТ ≥30 або ≥27 з принаймні одним супутнім захворюванням, пов'язаним з вагою, були рандомізовані для отримання плацебо або ретатрутиду (1 мг, 4 мг з двома схемами титрування, 8 мг з двома схемами титрування або 12 мг), що вводилися один раз на тиждень шляхом підшкірної ін'єкції протягом 48 тижнів.первинна кінцева точкабула відсоткова зміна маси тіла через 24 тижні, з вторинними кінцевими точками, що включали зміну ваги через 48 тижнів та категоріальні пороги втрати ваги (≥5%, ≥10%, ≥15%).
Ключові результати
-
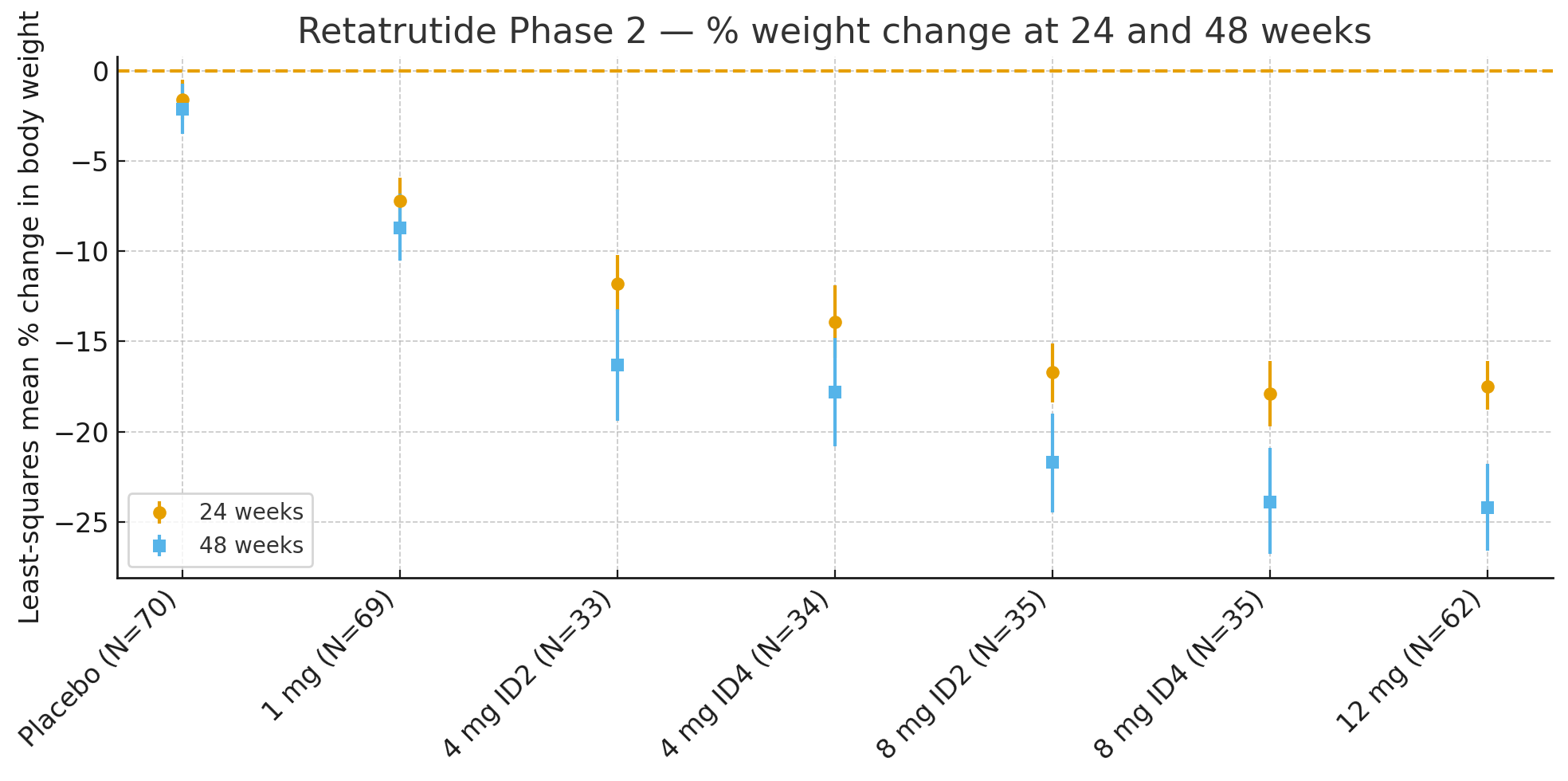
24 тижніСередня відсоткова зміна маси тіла відносно початкового рівня, визначена методом найменших квадратів, становила
-
Плацебо: −1,6%
-
1 мг: −7,2%
-
4 мг (разом): −12,9%
-
8 мг (разом): −17,3%
-
12 мг: −17,5%
-
-
48 тижнівВідсоткова зміна маси тіла була
-
Плацебо: −2,1%
-
1 мг: −8,7%
-
4 мг (разом): −17,1%
-
8 мг (разом): −22,8%
-
12 мг: −24,2%
-
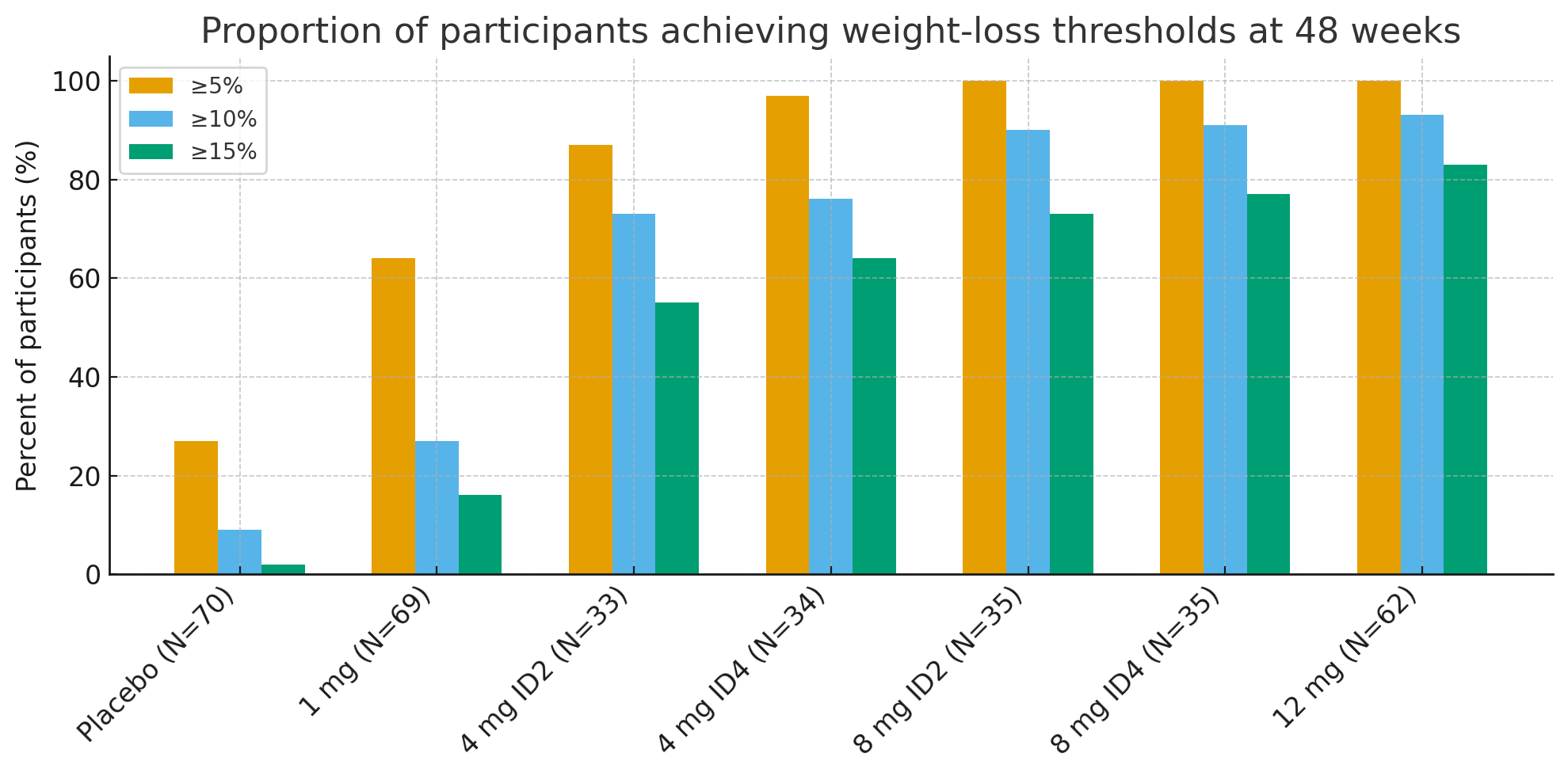
Через 48 тижнів частка учасників, які досягли клінічно значущих порогів втрати ваги, була вражаючою:
-
Втрата ваги ≥5%: 27% у групі плацебо проти 92–100% у групах з активним лікуванням
-
≥10%: 9% у групі плацебо проти 73–93% у групах з активним препаратом
-
≥15%: 2% у групі плацебо проти 55–83% у групах з активним препаратом
У групі 12 мг, до26% учасників втратили ≥30% своєї початкової ваги, що за величиною може бути порівнянно з баріатричною хірургією.
Безпека
Найпоширенішими побічними ефектами були шлунково-кишкові (нудота, блювання, діарея), зазвичай легкі або помірні та дозозалежні. Нижчі початкові дози (титрування 2 мг) зменшували ці ефекти. Спостерігалося дозозалежне збільшення частоти серцевих скорочень, яке досягло піку на 24-му тижні, а потім знижувалося. Частота припинення прийому препарату коливалася від 6 до 16% в активних групах, що дещо вище, ніж у групі плацебо.
Висновки
У дорослих з ожирінням без діабету щотижневе підшкірне введення ретатрутиду протягом 48 тижнів призводило досуттєве, дозозалежне зниження маси тіла(до ~24% середньої втрати при найвищій дозі), а також покращення кардіометаболічних маркерів. Побічні ефекти з боку шлунково-кишкового тракту були частими, але їх можна було контролювати за допомогою титрування. Ці результати фази 2 свідчать про те, що ретатрутид може стати новим терапевтичним еталоном для лікування ожиріння, що очікує підтвердження у більш масштабних, довгострокових дослідженнях фази 3.
Час публікації: 28 вересня 2025 р.