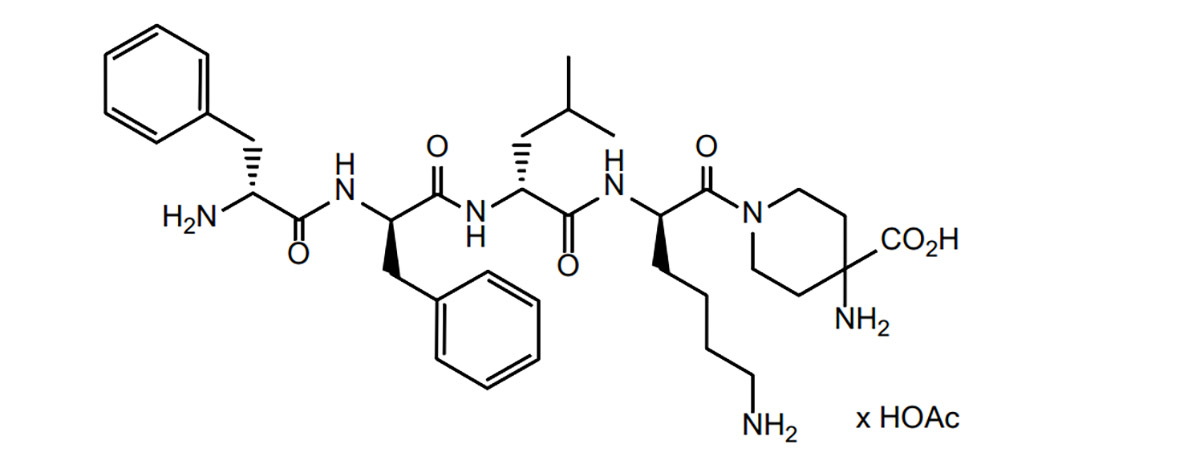
Ще 24 серпня 2021 року компанія Cara Therapeutics та її бізнес-партнер Vifor Pharma оголосили, що її перший у своєму класі агоніст каппа-опіоїдних рецепторів дифелікефалін (KORSUVA™) був схвалений FDA для лікування пацієнтів із хронічною хворобою нирок (ХХН) (позитивний помірний/сильний свербіж при лікуванні гемодіалізом), його вихід на ринок очікується у першому кварталі 2022 року. Cara та Vifor підписали ексклюзивну ліцензійну угоду на комерціалізацію KORSUVA™ у Сполучених Штатах та домовилися продавати KORSUVA™ компанії Fresenius Medical. Серед них Cara та Vifor мають 60% та 40% частки прибутку від продажів, окрім Fresenius Medical; кожна має 50% частки прибутку від продажів Fresenius Medical.
Свербіж, пов'язаний з ХХН (ХХН-аП), – це генералізований свербіж, який виникає з високою частотою та інтенсивністю у пацієнтів із ХХН, які перебувають на діалізі. Свербіж виникає приблизно у 60%-70% пацієнтів, які перебувають на діалізі, з яких 30%-40% мають помірний/сильний свербіж, що серйозно впливає на якість життя (наприклад, погана якість сну) та пов'язане з депресією. Раніше не було ефективного лікування свербежу, пов'язаного з ХХН, і схвалення Дифелікефаліну допомагає вирішити величезну проблему медичних потреб. Це схвалення ґрунтується на двох ключових клінічних випробуваннях фази III, що знаходяться у заявці про нерозголошення: позитивних даних випробувань KALM-1 та KALM-2 у США та в усьому світі, а також підтверджуючих даних 32 додаткових клінічних досліджень, які демонструють, що КОРСУВА™ добре переноситься.
Нещодавно надійшли гарні новини з клінічного дослідження дифелікефаліну в Японії: 10 січня 2022 року Cara оголосила, що її партнери Maruishi Pharma та Kissey Pharma підтвердили використання ін'єкцій дифелікефаліну в Японії для лікування свербежу у пацієнтів на гемодіалізі. Клінічні випробування III фази. Первинна кінцева точка була досягнута. 178 пацієнтів отримували 6 тижнів дифелікефаліну або плацебо та взяли участь у 52-тижневому відкритому розширеному дослідженні. Первинна кінцева точка (зміна балу за шкалою числової оцінки свербежу) та вторинна кінцева точка (зміна балу за шкалою тяжкості Шіраторі) значно покращилися від початкового рівня в групі дифелікефаліну порівняно з групою плацебо та добре переносилися.
Дифелікефалін – це клас опіоїдних пептидів. Виходячи з цього, Інститут досліджень пептидів вивчив літературу про опіоїдні пептиди та узагальнив труднощі та стратегії використання опіоїдних пептидів у розробці ліків, а також поточну ситуацію з розробкою ліків.
Час публікації: 17 лютого 2022 р.